速報)中国食品薬品検定研究院が「化粧品原料使用情報」を含む意見募集稿を通知。2,250成分で安全性のエビデンスとできる過去使用量がリスト化されました。
中国食品薬品検定研究院が「化粧品安定性評価技術ガイドライン(意見募集稿)」等の通知を公表
2024年4月10日、「化粧品安定性評価技術ガイドライン(意見募集稿)」等の通知を発表しました。
意見募集期間は2024年4月17日まで、発表された意見募集稿は起草説明含め以下7本です。
添付1.「化粧品安定性評価技術ガイドライン(意見募集稿)」及び起草説明
添付2.「化粧品防腐剤チャレンジ試験技術ガイドライン(意見募集稿)」及び起草説明
添付3.「化粧品包装材料適合性評価技術ガイドライン(意見募集稿)」及び起草説明
添付4. 「皮膚感作性適用試験評価策略応用技術ガイドライン(意見募集稿)」及び起草説明
添付5.「権威機関の化粧品安全性評価データ索引(意見募集稿)」
添付6.「化粧品原料使用情報(意見募集稿)」
添付7.「化粧品原料の使用に関する情報(意見募集稿)」起草説明

注目のポイント
今回の通知は中国食品薬品検定研究院が5月1日からの化粧品安全性評価報告書(完全版)移行に関する追加措置として、3月29日、4月4日に続く第3弾となります。
第1弾:3月29日「化粧品を3つに分類し、自己審査を導入」(https://wwip.co.jp/20240330-2)「化粧品リスク物質の特定と評価技術ガイドライン」(https://wwip.co.jp/20240331-1/)
第2弾:4月4日「「化粧品原料データ使用ガイドライン」」(https://wwip.co.jp/20240403-2/)
第3弾では、昨年来、期待され、公表時期が注目されていた、成分ごとの過去最高使用量リストが公表されました。(添付6)また、あわせて成分リスト中でCIR等の権威ある機関が公表している安全性文献が存在する成分をリスト化したデータ(添付5)も公開されました。
当局は、既使用原料目録に収載されている原料について、以下のように安全性エビデンスの参照方法を考えています。
① 中国化粧品安全技術規範を参照する成分(約800成分)
② 海外の権威ある機関が発行する安全性文献がある成分(3,572成分)(本通知の添付5)
③ 当局が、上記に該当しない原料について過去実績数値をリスト化(2,250成分)(本通知の添付6)
結果、合計で約6,600成分に何らかの安全性を示すことができるようになったため、ひとまず昨年から様々な議論を呼んだ原料安全性エビデンスの示し方についてある程度、先が見えたと言えます。
今回、WWIPでは、一番の注目である「6.化粧品原料使用情報(意見募集稿)」の概要についてお知らせ致します。
今回発表されたリストには、以下のように「中文成分名」「英文INCI名」の他、「使用部位(全身皮膚、顔、眼部等)」「使用方法(Leave on/Rinse off)」「使用量」が記されており、製品の使用部位や使用方法によって参照できる配合量が異なっています。
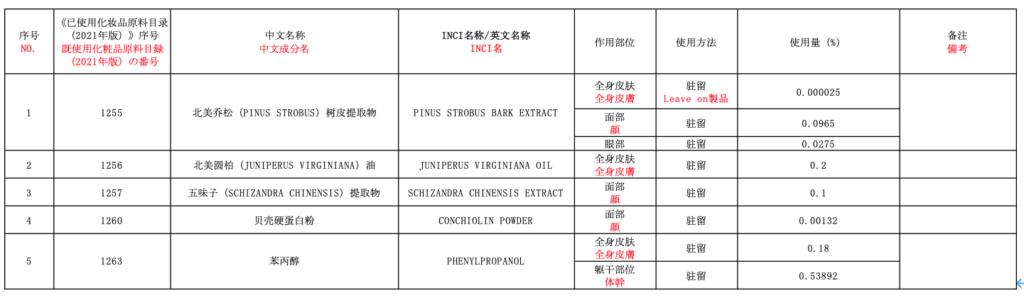
また、リストには以下の注意書きがあります。
1. 本原料使用情報は、我が国で現在有効な特殊化粧品に使用された原料の使用状況を客観的に収集したものであり、「化粧品安全技術規範」には含まれておらず、かつ権威ある機関からの評価報告書もありません。
リストアップされた原料の安全性の体系的な評価は未だ組織化されていないため、化粧品登録者および登記者は、関連する原料情報を使用する際に、関連する国内法、規制、基準、規格の関連要件を遵守して化粧品の安全性評価を行い、製品の品質と安全性に責任を負う必要があります。
2. 指定された原料の配合量は、化粧品の安全性評価の参考となるため、化粧品登録者及び登記者は、製品の使用方法や使用部位に応じて、原料の配合量を正しく使用する必要があります。
3. 同じ使用部位で同じ原料がLeave on製品の原料使用量のみ記載されている場合、Rinse off製品はLeave on製品の原料使用量を参照して使用することができます。
- 同じ使用部位で同じ原料を使用している場合、(一)全身皮膚、体幹部位、顔、口唇、眼部、(二)全身皮膚、体幹部位、手足、頭部、頭髪の順に2種類の場面で使用量を参照できます。
後ろの使用部位は、前の使用部位で使用された原料投入量を参照することができますが、製品の使用部位が眼部で、他の列記された使用部位での使用量を参照する際には、別途、原料の眼刺激性も評価する必要があります。
※文意を取りづらいので、以下の通り弊社解釈を説明致します。
同じ使用部位に使用する同一原料の場合、以下2パターンに記載された使用部位の順に安全性データを参照できます。
(1)全身皮膚、体幹部位、顔、口唇、眼部 →例:スキンケア、メイクアップ製品等
(2)全身皮膚、体幹部位、手足、頭部、頭髪→例:シャンプー、コンディショナー製品等
(1)(2)いずれの場合も全身皮膚、次いで体幹部位は暴露量が多く安全性リスクが高いため、そのデータがあれば他の部位に使用する製品の安全性評価材料として参照可能であるということです。
そのため、例えば顔に使用するスキンケア製品の場合、全身皮膚のデータがあれば安全性データとして参照可能です。
ただし、(1)のパターンで使用部位が眼部の場合、”全身皮膚、体幹部位、顔、口唇”のデータを参照できますが、その場合は原料の眼刺激性も別途評価する必要があります。
WWIPコメント
中国食品薬品検定研究院は4月3日に「化粧品原料使用ガイドライン」の意見募集稿を発表しており、化粧品成分を安全性評価をするための材料の1つに「化粧品監督管理部門が公布する原料使用情報」というものがありましたが、これが今回発表されたリストを指すと考えられます。(以下、弊社リリース参照)https://wwip.co.jp/20240403-2/
今年の5月以降、「化粧品安全性評価報告書<完全版>」の要求が開始され、「既使用化粧品原料目録(2021年)」に収載されていた“最高歴史使用量”は参照できなくなります。今回発表された“化粧品原料使用情報”中の“使用量(%)”と“最高歴史使用量”を比較すると、今回発表されている使用量の方が少なくなっている(厳しくなっている)箇所も散見されますが、今回の参照データだけでも、評価根拠が増えることは企業にとって朗報であるといえます。今後のNMPAの正式な確定ルールの発表に要注目です。
中国語の原文ダウンロードはこちら
<本件に関するお問い合わせ>
株式会社WWIPコンサルティングジャパン
TEL :03-6206-1723
Email:official@wwip.co.jp