中国健康食品(中国語:保健食品)の申請について
日本で食品を健康食品として販売するのに、栄養機能食品または特定保健用食品の許認可を消費者庁から取得すると同様、同じような商品を中国で販売するにも関連の申請が必要です。

中国健康食品(保健食品)の審査認可制度の歴史的沿革
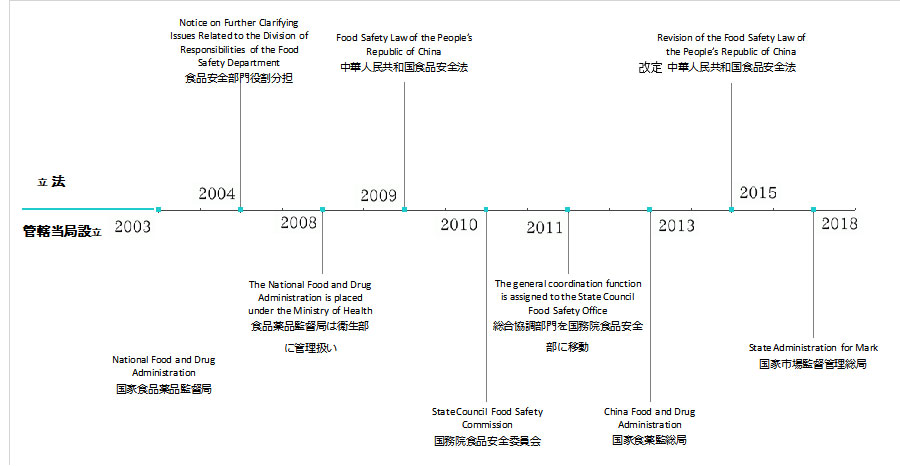
短期間に管轄機関が変更され、法規定も改定されているが、その背景には3つを方針がある
- 緩和 従来の厳しすぎた規制を緩める
- 管理 管理体制整備
- サービス拡充
かつて保健食品は医薬品・化粧品などと同様、CFDA(国家食品薬品監督管理局)で申請を扱っておりましたが、2018年年末中国当局の組織変更により、CFDAはNMPA(国家薬品監督管理局)へ機能移行し、医薬品や化粧品はNMPA申請となりました。

登録されると、登録番号が発行され、製品には、通称「青帽子」と呼ばれる保健食品としての認定マークを貼付することができます。
同時に、食品の申請と審査はNMPAではなく、上位組織のSAMR(国家市場監督管理総局)で行う事になりました。
* 尚、日本でも医薬品・医療機器・化粧品はPMDA、保健食品は消費者庁で、それぞれ別の機構で承認を受けています。
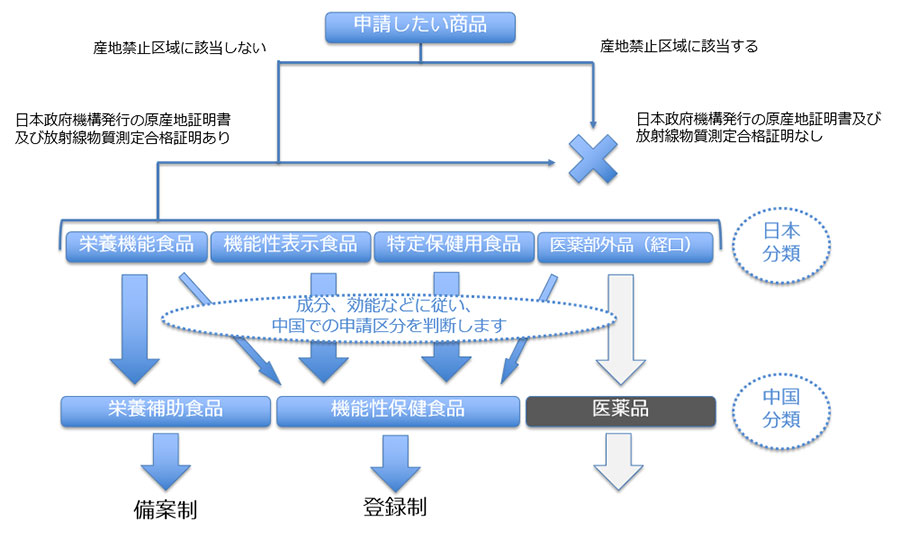
保健食品の分類と申請方法
中国における健康食品(保健食品)とは?
保健食品は「機能性保健食品」「栄養補助食品」の2つに分けられます。保健食品を一般貿易で輸出する場合には、事前の登録手続きが必要です。
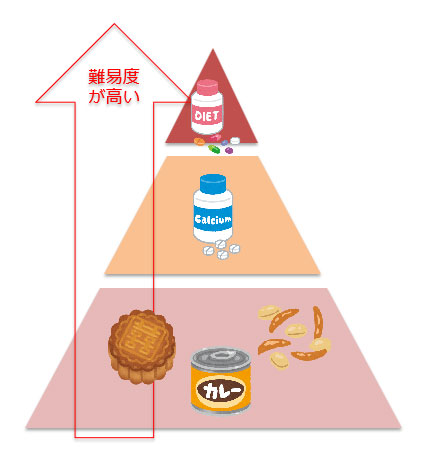
機能性保健食品(中文:功能性保健食品)
高度な機能性を謳う食品/機能性成分を含む食品
最も難易度の高い保健食品申請が必要。
栄養補助食品(中文:栄養補助食品)
「ビタミンC配合」などの栄養補充を謳える食品、備案方式での保健食品申請が必要。
※ 申請時に該当成分の含有率が一定以上であることが要求される
一般食品(広義の普通健康食品を含む)
効能のない普通の食品、保健食品申請は必要なし。
※ 制度としての分類はないが、一般的に以下のようは製品を含む
功能性食品/特殊用途食品/栄養補助食品/療効食品/緑色食品/一般食品
ここでいう「栄養補助食品」は成分が添加されていればよく含有率の要求はない。
栄養補助食品
栄養補充を目的とする食品。補充される栄養成分は決められている:
ビタミンA、ビタミンB1、ビタミンB2、ビタミンB6、ビタミンB12、ビタミンC、ビタミンD、ビタミンE、ビタミンH、ビタミンK、ビタミンM、ニコチン酸、コリン、パントテン酸、Ca、Mg、K、Mn、Fe、Zn、Se、Cu
機能性保健食品
医薬品の様に病気を治療する目的ではなく、あくまで下記の各効能にて身体調整を行う目的とする食品:
血中脂肪降下、血圧降下、抗酸化、記憶力増強、目の疲労抑制、鉛排出、喉ケア、睡眠改善、乳分泌促進、疲労改善、酸素不足耐性改善、放射線被害保護作用、ダイエット、成長サポート、骨密度改善、栄養性貧血改善、化学性肝障害保護作用、ニキビ改善、しみ改善、皮膚水分改善、皮膚油分改善、消化機能改善、便秘改善、胃粘膜障害保護作用、腸内細菌の調整、免疫力改善。
*あくまで身体調整のサポートであり、治療効果ではありません。
申請方法の違い
保健食品備案 = 栄養補助食品
保健食品生産企業が法定手順や条件と要求に基づいて、製品の安全性、保健機能と品質制御性を明らかにした資料を食品薬品監督管理部門に提出し、記録として保存され、公開され、保管される過程を指す。
所要時間:約6~12ヶ月(検査期間を含む)
保健食品登録 = 機能性保健食品
食品薬品監督管理部門が、登録申請者の申請により、法定手順や条件と要求に基づいて、登録申請した保健食品の安全性、保健機能と品質制御性などの関連する申請資料に対して、系統的な評価と審査を行い、その登録を許可するかどうかを審査し認可する過程を指す。
所要時間:約1~2年(検査期間を含む)
健康食品(保健食品)の登録状況
2016.7.1に備案登録制度が開始された。その年は全体で348件(国内344件・海外4件)と登録件数が落ち込んだ。
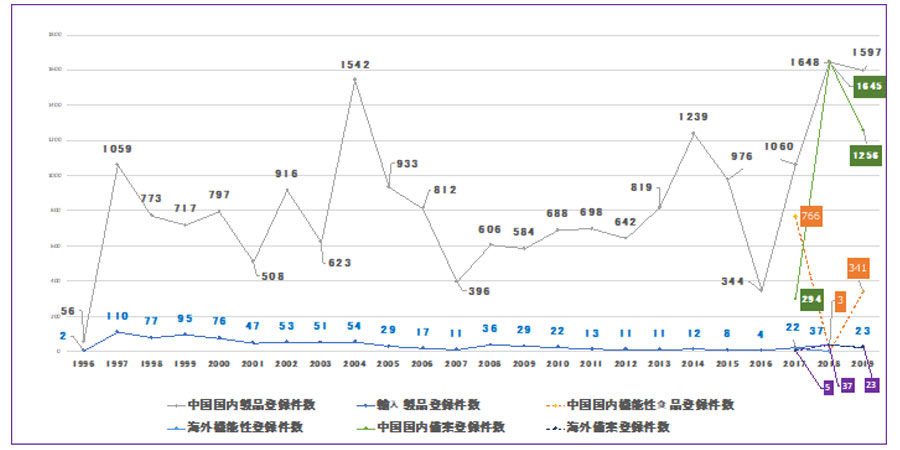
- 2017年は、1082件が(1060+22)登録 (国内機能766件・国内備案294件・海外機能17件・海外備案5件)
- 2018年は、1653件(1648+37)と登録が急増(国内機能3件 ・国内備案1645件・海外備案5件)
- 2019年は、1620件(1597+23)の登録 (国内機能341件・国内備案1256件・海外備案23件)
2016年の備案制度開始以降、全体の大きな割合を備案制度の対象である栄養補助食品が占めていることがわかる。
機能性保健食品登録状況
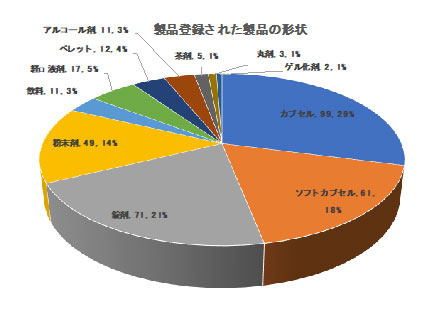
登録健康食品の剤形は、カプセル、ソフトカプセル、錠剤、粉末剤、飲料、経口液剤、ペレット、アルコール剤、茶剤、丸剤およびゲル化剤を含む。
このうちカプセル、錠剤、ソフトカプセル、粉末剤が相当数を占める。
承認された健康食品のうち、免疫力を高める健康食品の数が最も多い。
次いで、疲労を緩和、骨密度の増加、睡眠の改善、記憶改善、抗酸化、化学肝障害の補助保護機能、低酸素耐性の改善、便通、体重減少、カルシウム補充など。
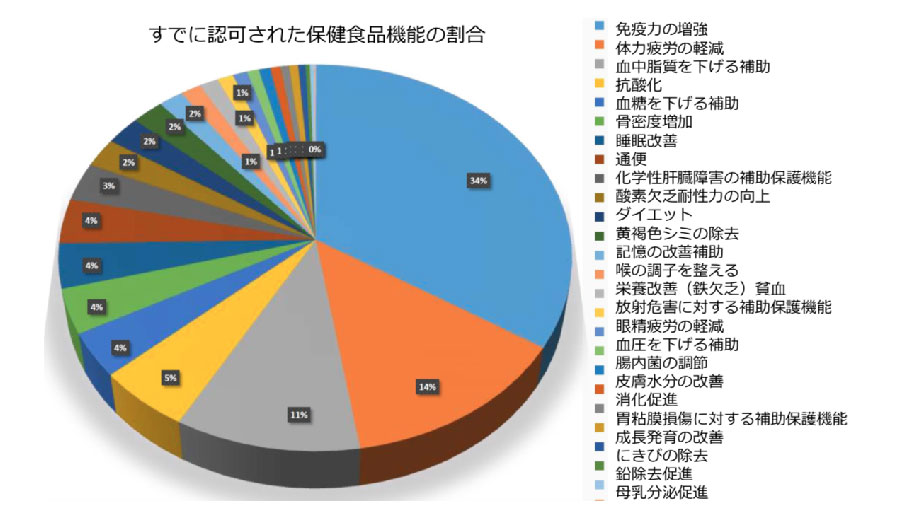
栄養補助食品登録状況
国産および輸入健康食品の備案申請の全体像
2017年7月27日、広東省食品医薬品局が初の国産栄養補助食品の
備案登記を発表した。
※ 備案申請は、地方当局に国内の栄養補助食品、 国家局に輸入栄養補助食品を申請する。2021年1月末日現在、125件の輸入健康食品が登記されている。
2021年3月1日より中国栄養補助食品の原料目録が改定、施行される。従来の目録に修正を加えた新しい目録が発表、中でもコエンザイムQ10をはじめとする5種類の原料が目録に新たに収載されたことが注目されている。WWIPでは、以下の11文書の翻訳を行い発表。詳細、資料ダウンロードは以下関連資料を参照。
関連資料:中国保健食品新目録について
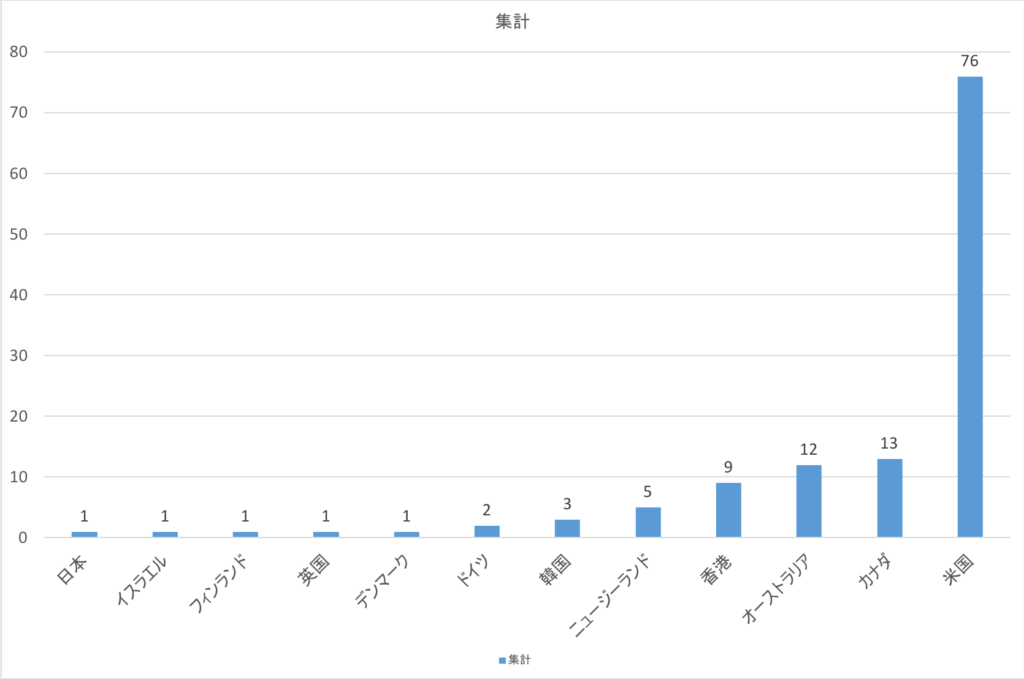
輸入健康食品の備案申請(国別)
125件の輸入栄養補助食品備案申請の内訳は、
米国、カナダ、香港、ニュージーランド、オーストラリア、韓国、英国、
イスラエルの8カ国。内34件の備案申請が米国企業。
英国とイスラエルは、2019年に初の備案申請を取得。
現時点で輸入製品の備案登録件数はまだ少ないが、備案制度が2018年以降、機能し始めている点と、備案制度は従来申請に比べ大きくハードルが下がっていることから、日本企業も積極的に利用すべきだと考えている。
健康食品(保健食品)申請実務
〜栄養補助食品(備案申請)〜

- 中華人民共和国食品安全法
- 保健食品の登録と備案に関する法規定
- 《保健⾷品の登録と備案に関する管理方法》
- 《保健⾷品の登録審査と認可に関する作業細則》
- 《保健食品の登録申請サービス指針》
- 《保健食品の備案作業指針》
- 《保健食品の備案製品に関する主な⽣産⼯程(試⾏)》
- 《保健食品の備案製品で使⽤できる補助原料及び使⽤規定(試⾏)》 《保健食品原料目録(⼀一)》
- 《保健食品の公示された認可保健機能目録(⼀一)》
- 《保健食品の機能⽬録と原料⽬録管理方法》の制定
- 生産経営許可に関する法規定
- 《食品⽣産許可管理⽅法》
- 《食品経営許可管理方法》
- 《食品⽣産許可審査通則》
- 《食品経営許可審査通則(試⾏》
- 《保健⾷品生産許可審査細則》
- 生産経営と日常監督検査に関して
- 《食品の⽣産経営と日常監督の検査管理方法》および保健⾷品生産企業の日常監督検査表
申請可否の判断
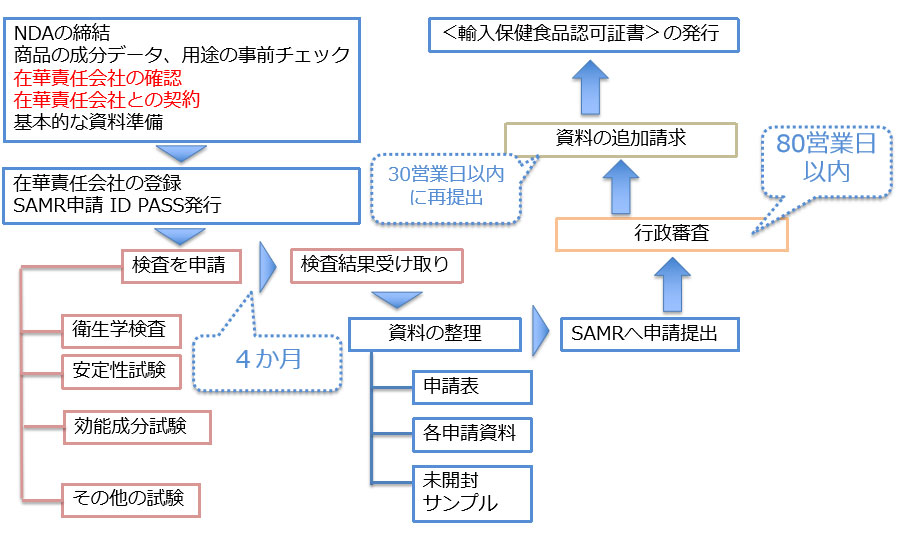
申請の流れ
申請必要書類(例)
- 保健食品備案登記表・誓約書
- 申請会社の登記証明書類
- 配合原料資料
- 生産プロセス
- 安全性及び保健機能評価資料(3ロット分の検査データ)
- 食品包装材料の種類・名称・標準(食品と接触する包装素材とその安全性等)
- 製品の日本のパッケージ資料と中文ラベル
- 製品技術要求 (感覚器指標など)
- 検査報告書(サンプル検査後に受け取る報告書)
- 販売実績証明(日本における1年以上の販売実績が必要)
- 日本の保健食品関連標準を示す資料(取得特許、文献資料等あれば)
- その他必要に応じた補足資料
健康食品(保健食品)の成分チェック
申請を検討する前に、まず成分チェックが必要です。
成分チェックを行うことで、「製品の市場流通が可能か否か?」、「可能な場合、申請が必要か?」 が判断できます。
- 一般食品として通関できる
- 栄養補助食品としての申請が必要
- 機能性食品としての申請が必要
- 成分の中に、使用が禁止された成分がある(成分を変えないと中国市場で流通できない)
詳しくはお問い合わせください。
成分チェックシート
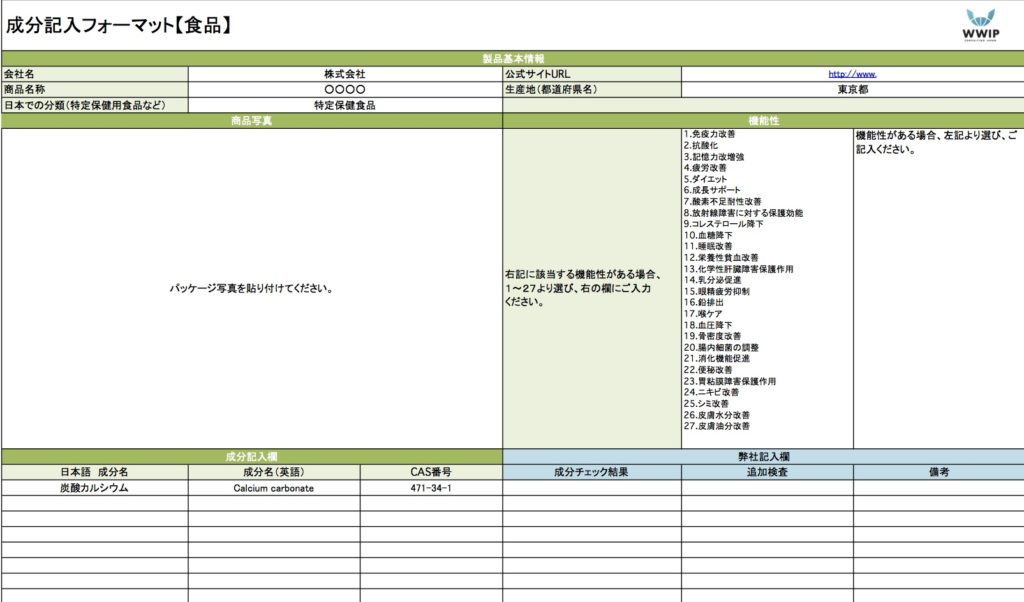
このシートに製品情報、成分の日本語名と英文名、CAS番号を記入して頂きます
成分チェック結果
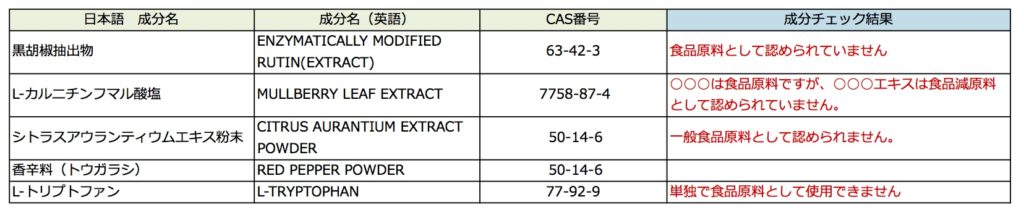
成分チェックをご依頼頂く場合はこちらから、成分チェック依頼フォームに必要事項、製品データ等をアップロードしてください
* 内容はダミーです
健康食品(保健食品)に関するQ&A
- プラセンタエキス100%(ブタorウマ)の粉末食品は、分類上「機能性保健食品」「栄養補助剤」「普通健康食品」「一般食品」のどちらに当てはまりますか?
-
中国の食品に関する分類は、保健食品と一般食品に分かれ、保健食品は、機能性保健食品と栄養膳食補充食品に分かれます。
現在の中国では動物プラセンタを普通食品原料として使用することは禁止されています。また、同じ動物でも羊については、2008年には、中国衛生部より「羊プラセンタを普通食品原料として使用することを禁止する通達」(衛監督函〔2008〕322号)を配布し、羊プラセンタの使用に関しては明確に一般食品として使用できない旨を表明しています。
ブタ、ウマのプラセンタエキス100%の粉末食品については、明解な禁止規定はないものの、「一般食品」と「栄養補助食品」では使用できず、「機能性保健食品」となります。 - ハードカプセル・ソフトカプセル・打錠の健康食品の分類を教えてください。
-
健康食品か医薬品かの分類は、食品の包装(カプセルか錠か等)によらず、中身で判断されます。
- プラセンタエキス末(ブタorウマ)配合のゼリー剤は、許認可をとれる可能性はありますか?(参考)JBPプラセンタゼリー ピュア
-
現在、中国のSAMR(国家市場監督管理総局)の栄養食品分野の申請は非常にハードルが高く、特に機能性保健食品の申請は停滞しており、数年間店晒しの申請も多く見受けられます。
仮に、こうした申請が進み始めたとしてもプラセンタエキスに関しては粉末でも、液体でも、機能性を宣伝する新原料保健食品の申請という非常にハードルが高い申請となります。 - ブタプラセンタエキス末、ブタプラセンタエキス液体、ウマプラセンタエキス末、ウマプラセンタエキス液体の(許認可申請時に都合の良い)英語表記名
-
粉末についてはPlacental extract (Lyophilized powder)がお勧めです。商品説明にブタまたはウマ由来と明記する必要があります。
液体についてはplacental extract(hydrolyzate)がお薦めです。
これも商品説明にブタまたはウマ由来と明記する必要があります。
※ こちらは生産プロセスで左右されるので、水で溶かして生成した
液体の場合にはplacental extract(hydrolyzate)、
生産プロセスで干して作成した粉末の場合には、Placental extract (Lyophilized powder)をお勧めしています。
中国向けの健康食品申請に関する更に詳細な資料(申請プロセス、必要資料など)は、こちらから資料を取得してご参照ください。

弊社には申請代行のみならず、専門的なご質問に調査、回答するコンサルティングサービスも行っております。今すぐに中国へ製品を進出する予定はないが、将来には…という会社様、及び中国向けの製品を開発している会社様など向きのサービスになっております。









