【速報!】中検院発表「化粧品原料データ使用ガイドライン」意見募集稿のお知らせ
2024年4月3日、中検院(中国食品薬品検定研究院)が表題のガイドラインの意見募集稿と起草説明を発表しました。意見募集の締切りは4月10日(水)です。
原文PDFデータ:
1)今回の発表の背景
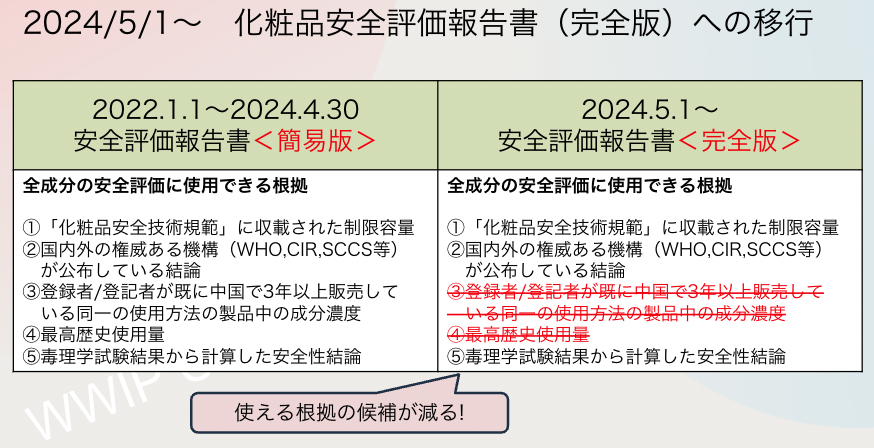
5月以降に中国国家薬品監督管理局(NMPA)で化粧品申請を行う企業は「化粧品安全評価報告<完全版>」を要求されます。当該完全版のレポートで必要となる“成分ごとの安全性評価”については、4月末まで要求される「化粧品安全評価報告<簡易版>」よりも評価根拠として使える候補が非常に少なくなるため、中国国内で緩和措置を求める声が多く挙がっています。
2024年3月29日には「化粧品安全評価資料提出ガイドライン」の意見募集稿(以下リリース参照)も発表されましたが、申請企業にとってさほど条件が緩和される内容ではないため、追加措置の発表に期待したいところです。


2)今回発表された通知の注目ポイント
注目ポイントは以下の通りです。
成分の安全評価根拠の候補
下記マーカーを引いた箇所が根拠材料として追加されています。
①「化粧品安全技術規範」に収載された制限容量(防腐剤の制限容量リスト等)
②権威ある化粧品安全評価機関によって公布された評価結論
③国内外の権威ある機関(WHO,FAO等)が公布している安全限界量または結論
④化粧品監督管理部門が公布する原料使用情報
⑤国内外の3年以上の成分の使用実績
⑥成分の安全な食用履歴
⑦構造と性質が安定した高分子ポリマー(生物活性の高い原料を除く)
④化粧品監督管理部門が公布する原料使用情報
「化粧品監督管理部門が発表する原料使用情報が評価の参考となる」とだけ記されており、現段階では内容が曖昧なので追加発表に期待したいところです。
⑤国内外の3年以上の成分の使用実績
中国国内だけでなく海外での使用実績も認められる点は朗報ですが、以下の通り複数の条件付きです。
●同じ原料番号かつ原料中の主要効能成分の含有量と溶剤が一致していること。
●申請する製品の対象成分の含有量が、3年以上使用実績のある成分含有量より低いこと。
●販売実績ある対象市販製品によって生じた不良反応の分析結果が、対象原料の安全性に関わらないこと。
●“成分の過去の使用量を相互参照することができて、暴露量が高く接触時間の長い製品”は、“暴露量が低く接触時間が短い製品”の評価に用いることができる。ただし、使用対象者グループ・使用部位・使用方法等の角度から十分に分析し、その合理性を説明する必要があり、必要に応じて局所毒性評価を行う必要がある。
また、自社または授権された他社の同一原料の3年以上の使用実績を証明するため以下の資料が必要です。
1.原料中の主要効能成分の含有量と溶剤の関連資料
2.原料含有量の証明
NMPA登録済みの特殊化粧品:登録証書と登録処方(NMPA申請した処方と一致している必要あり)
NMPA登記済みの普通化粧品と海外で販売されている化粧品:原料含有量が記載されているまたは原料含有量を計算できる生産投入記録と登記証明書(海外販売のみ行っている場合は不要)
3.不良反応モニタリング状況の説明
4.市場販売データの証明資料
末端小売販売数量を基準とする場合は、3年間の累計販売数量10,000個以上
化粧品メーカーの工場出荷数量を基準とする場合は、3年間の累計工場出荷数量30,000 個以上
同じグループ会社が同じ原料を使用している製品の販売数量は、合わせて計算することが可能だが、併せて暴露量と接触時間について説明する必要あり
5.他社の市場販売データを証拠とする場合
原料生産企業あるいは同一原料を使用した化粧品会社が発行した授権書を提出すること
6.その他の関連資料
例外規定
1.シミ取り美白の有効成分として使用される成分
「④化粧品監督管理部門が公布する原料使用情報」「⑤国内外の3年以上の成分の使用実績」を安全性評価根拠として使用不可。
2.抜け毛防止、ニキビ除去(ニキビ軽減)、抗シワ(物理的抗シワを除く)、フケ防止、消臭の有効成分として使用し、かつ生物活性の高い特性をもつ成分
「⑤国内外の3年以上の成分の使用実績」は安全性評価根拠とできるが、「④化粧品監督管理部門が公布する原料使用情報」は使用不可。
3)WWIPより
まだ意見募集稿の段階なので確定ではありませんが、多少は安全評価材料の候補の幅が広がろうとしている気配があるものの、5月以降にNMPA申請を行う企業にとっては正直今ひとつかと思います。願わくば「化粧品安全評価報告<簡易版>」で使用が認められていた“最高歴史使用量”(NMPAが2021年に発表している、中国で過去使用された成分濃度)も根拠の1つとして認めてほしいところですが、そこまで認めると<簡易版>との差がなくなるため難しいかと思います。
今回の発表で登場した「④化粧品監督管理部門が公布する原料使用情報」は具体的な内容が明らかになっていないので、このあたりの内容含め、今後のNMPAの発表に注目です。
4)WWIP開催セミナーのお知らせ(再掲)
化粧品・化粧品原料に関するNMPA最新情報をお届け!是非ご参加ください!
4/17(水)「中国化粧品新原料登録・登記 基礎解説」セミナー

4/23(火)「中国化粧品広告関連規制と NMPA最新情報」セミナー

<本件に関するお問い合わせ>
株式会社WWIPコンサルティングジャパン
TEL : 03-6206-1723
Email: official@wwip.co.jp