12/8、化粧品NMPAシステム内で原料変更手続きに関する通知が表示されました
化粧品NMPA手続きは専用システムにログインして行います。
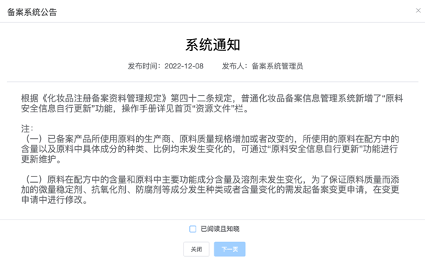
今回、NMPAシステム内で“登記済み化粧品の原料を変更する場合の手続き”に関する短い通知が表示されました。
1.表示概要
「化粧品登録登記資料管理規定」第42条の規定により、普通化粧品の登記情報管理システムは「原料安全情報自主更新」機能を新設。
注意:
(1)既に登記した製品に使用されている原料の製造会社は、原料品質規格が増加または変更された場合、使用している原料配合中の含有量、原料中の具体的な成分の種類、比率が変化していない場合は「原料安全情報の自主更新」手続きが可能。
(2)原料の配合中の含有量と原料中の主要効能成分の含有量及び溶剤には何も変更が生じていないが、原料の品質を保証するために添加する微量安定剤・抗酸化剤・防腐剤等の成分の種類あるいは含有量に変更が生じた場合は、登記変更申請書を提出し、変更申請書内に変更内容を記入すること。
2.関連法規と対象分類
「化粧品登録登記資料管理規定」第42条とは、原料変更手続きについて規定した条文です。(ページ下部参照)
この条文は「登録あるいは登記済み製品」、つまり特殊化粧品と普通化粧品の両方を対象としたものですが、今回のシステム上の表示内容は“普通化粧品の登記情報管理システム”だけに表示された、普通化粧品向けの案内です。
ただし、特殊化粧品は原料変更手続きできないという意味ではありません。恐らく、特殊化粧品と普通化粧品の管理システムが分かれているため、このように先行して普通化粧品のシステムを構築してその手続きについて表示したに過ぎず、今後特殊化粧品のシステムの方にも同様の案内が出るのではないかと思われます。
3.変更手続きの難易度
NMPAは基本的に「処方が変われば別製品」というスタンスであるため、このような僅かな変化でない限り、イチから申請手続きをやり直さなければなりません。
(1)は原料の組成が同一のものであり、「自主更新」すなわち“審査なし”で更新手続きできるということを意味しますので、比較的容易であると言えます。
(2)の場合は僅かな変化しか認められず、変更手続き後に審査が行われます。 使用している原料の廃盤、製品のリニューアル等による処方変更はよく起こることですが、このような原料変更手続きの条件に合致しない場合、中国展開のために苦労して許可取得した製品を「再申請/再登記」しなければならなくなる可能性があるため、注意が必要です。

<本件に関するお問い合わせ>
株式会社WWIPコンサルティングジャパン
TEL : 03-6206-1723
Email: official@wwip.co.jp