【中国化粧品NMPA】「2024年第50号公告」に対する解釈を明示。広州市市場監督管理局が普通化粧品登記に関するQ&A(第六十二回)を公表
2024年6月4日、広州市場監督管理局(SAMR局)が普通化粧品登記Q&A(第六十二回)」(以下「第六十二回Q&A」)を公表しました。株式会社ワールドワイド・アイピー・コンサルティングジャパン(以下、WWIP) は、当該通知のうち、特に重要なポイントを抜粋しお知らせ致します。
原文: https://scjgj.gz.gov.cn/zwdt/tzgg/content/post_9686565.html
当該通知は先日弊社リリースしました以下の[中国NMPA「2024年第50号公告」の解釈が揺れている?NMPAの発表と動きに要注目]に関連する重要な内容です。その内容にフォーカスしご紹介いたします。

Q:化粧品の安全評価資料はどのように分類して管理しますか?
A:「化粧品安全性評価資料提出に関するガイドライン」の化粧品の分類に関する規定により、「分類規則」を参照し、化粧品効能訴求、対象使用者、製品剤形などのさまざまな側面での化粧品の分類に基づき、リスクレベルを総合的に考慮して、安全観測期間中の新原料やナノ原料等の高リスク原料の使用可否、機器或いは器具と併用することが必須か否か等の分類方式を追加し、且つ化粧品安全性評価資料中の重点的な注目すべき内容と組み合わせて、化粧品を2 つのカテゴリーに分類しています。
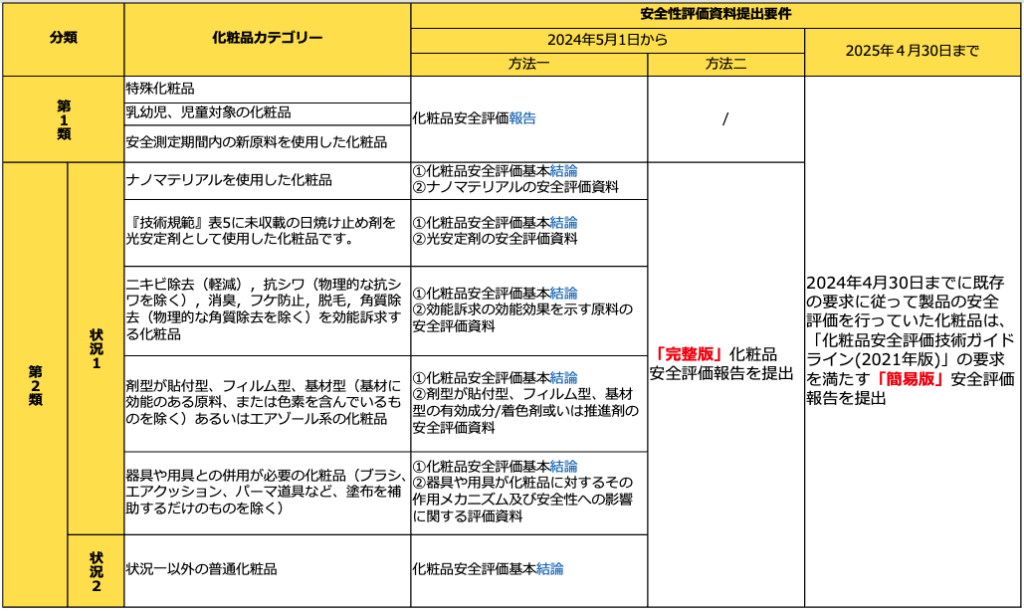
化粧品安全性評価資料は 2 つのカテゴリーと 2 つの状況に応じて相応する提出資料を選択します。第一類化粧品は化粧品安全性評価報告書を提出する必要があります。第二類化粧品は、化粧品安全評価報告書を完成することと、登記者の品質管理システムの運用が良好であることを前提として、状況一の化粧品の場合は化粧品安全性評価の基本結論と以下の表に適合するリスクポイントの安全性評価資料を提出することができます。状況二の化粧品の場合は、化粧品安全性評価の基本結論を提出することができます。また、第二類化粧品は直接に化粧品安全評価報告書の提出を選択することもできます。
同時に、化粧品の研究開発には一定の時間が必要であることを考慮し、企業の研究開発資源の重複投入を避けるため、『国家薬監督局の化粧品安全評価管理の最適化に関する公告』(2024年第50号)は、2024年4月30日までに既存の要求に従って製品の評価を展開した化粧品に対して1年間の猶予期間を設けました。2025年5月1日前までに、化粧品登録・登記者は化粧品の登録・登記を行う際に、「化粧品安全評価技術ガイドライン(2021年版)」の要求を満たす「簡易版」安全評価報告書を提出することができます。
2024年4月30日までに「簡易版」の要求に沿って安全評価を行っていた製品に限り、「簡易版」を提出可。この条件に合わない場合は「完整版」の対応が必要となる!
化粧品安全評価資料の分類管理
WWIPコメント
今回のQ&Aを通じて広州市場監督管理局の「2024年第50号公告」に対する解釈が明らかになりました。現時点では、安全評価の時期にかかわらず「簡易版」安全評価報告書を受理している地区もありますが、これから申請を検討される方は「完整版」安全評価報告書要求に従って中国N M P A化粧品登録・登記の準備をすべきかと考えます。
WWIPは今後も中国当局の動向をタイムリーにキャッチし、皆様に最新情報をお伝えるように努めて参ります。
WWIPでは、ニュースリリースに関する皆さまのご意見・ご感想を募集しております。いただいたご意見を踏まえ、より皆さまのニーズに合う情報をお届けできるよう努めて参りますので、以下ボタンよりお気軽に投稿ください。
<本件に関するお問い合わせ>
株式会社WWIPコンサルティングジャパン
TEL :03-6206-1723
Email: official@wwip.co.jp